Viện Vaccine và Sinh phẩm y tế (IVAC) là đơn vị thuộc Bộ Y tế, được thành lập năm 1978, có kinh nghiệm hàng chục năm nghiên cứu, sản xuất vaccine phục vụ chương trình tiêm chủng mở rộng và phòng chống bệnh truyền nhiễm. Với bề dày ấy, IVAC được kỳ vọng sẽ giúp Việt Nam từng bước tự chủ được vaccine phòng COVID-19. Vậy nên tin IVAC dừng thử nghiệm lâm sàng ứng viên vaccine Covivac gây nhiều xôn xao dư luận.
Covivac đang đối mặt với khó khăn gì?
Trả lời Pháp Luật TP.HCM, ông Dương Hữu Thái, Viện trưởng IVAC, giải thích Covivac đang trong thử nghiệm lâm sàng giai đoạn 2 nên vẫn tiếp tục thu thập dữ liệu như kế hoạch. Chỉ là việc xây dựng đề cương thử nghiệm giai đoạn 3 phải tạm dừng để điều chỉnh cho phù hợp với tình hình mới. “Trước đây chúng tôi dự kiến tháng 12 sẽ chuyển sang giai đoạn 3 nhưng giờ tuyển tình nguyện viên theo kế hoạch cũ khó quá” - ông Thái cho biết.
Ông Hoàng Hoa Sơn, Cục Khoa học Công nghệ và Đào tạo, Bộ Y tế, người theo dõi công tác nghiên cứu vaccine COVID-19, xác nhận Covivac gặp một số khó khăn nhưng thông tin dừng thử nghiệm lâm sàng là không đúng. “Thử nghiệm giai đoạn 2 chúng tôi vẫn đang đợi kết quả. Đề cương giai đoạn 3 đang trong quá trình xây dựng, chưa phê duyệt. Vậy nên không có chuyện dừng thử nghiệm, dù khó khăn là có thật” - ông Sơn nói.
Từ kinh nghiệm nghiên cứu, phát triển vaccine cúm A/H5N1 bằng công nghệ virus bất hoạt nuôi cấy trên trứng gà có phôi, chi phí thấp, IVAC khởi động dự án vaccine COVID-19 từ tháng 5-2020. Nhờ quan hệ quốc tế rộng rãi, đơn vị này tham gia một liên minh sản xuất vaccine COVID-19, do PATH (một tổ chức phi lợi nhuận của Mỹ) tài trợ.
Sau khi hoàn tất các thử nghiệm tiền lâm sàng, tháng 3-2021, Covivac bắt đầu thử nghiệm lâm sàng trên người giai đoạn 1, cho kết quả khả quan và đến cuối tháng 8 thì triển khai giai đoạn 2.
Nếu so với ứng viên Nano Covac của hãng sinh phẩm tư nhân Nanogen thì tốc độ triển khai của Covivac với nhiều ràng buộc thủ tục của nhà tài trợ Mỹ là khá chậm.
Tuy nhiên, Covivac lại kịp điều chỉnh đề cương giai đoạn 2, thay vì đối chứng bằng giả dược (placebo) mà Nano Covax đang áp dụng thì chuyển sang phương pháp so sánh đối đầu: Trong tình nguyện viên giai đoạn 2, một số thì tiêm Covivac, số còn lại đối chứng bằng tiêm vaccine nhập ngoại AstraZeneca cùng công nghệ.
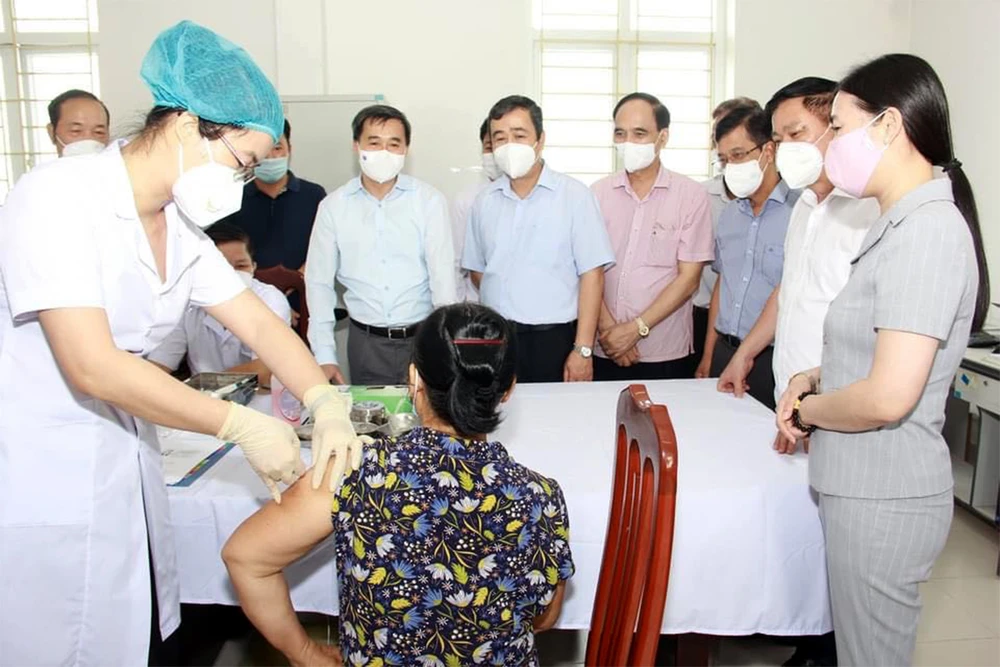
Tiêm thử nghiệm lâm sàng vaccine Covivac cho tình nguyện viên tại Trung tâm Y tế huyện Vũ Thư, tỉnh Thái Bình. Ảnh: VGP
Theo kế hoạch này, sau khi thử nghiệm giai đoạn 2 chứng minh được về tính an toàn, tính sinh miễn dịch và lựa chọn được liều tiêm thì tháng 12 này, Covivax sẽ xin phê duyệt đề cương giai đoạn 3, tiếp tục theo hướng so sánh đối đầu AstraZeneca. Vấn đề là phải tuyển một lượng lớn tình nguyện viên, như cách làm của Nano Covax giai đoạn 3 là 14.000 người, tuổi từ 18 trở lên và chưa tiêm vaccine COVID-19 nào.
Điều này là vô cùng khó khăn, khi mà số liệu cập nhật của Bộ Y tế đến ngày 30-11, cả nước đã tiêm tổng cộng 123.442.920 liều vaccine, trong đó tiêm mũi 1 là 71.736.491 liều, mũi 2 là 51.706.429 liều. Số người 18 tuổi trở lên chưa tiêm không nhiều và rải rác ở các địa phương.
Chưa kể, thử nghiệm lâm sàng giai đoạn 3 đòi hỏi một khoản đầu tư rất lớn mà viện nghiên cứu nhà nước như IVAC khó chủ động được.
“Giai đoạn 1, giai đoạn 2 chúng tôi tự lo được bằng các nguồn vốn khác nhau, có phần từ ngân sách, có phần tài trợ trong nước và cả nước ngoài. Còn tới đây tiếp tục thế nào thì các khó khăn chúng tôi đã báo cáo, chờ Bộ Y tế hướng dẫn. Tiềm lực tài chính mình không so sánh với bên ngoài được” - Viện trưởng Dương Hữu Thái cho biết.
Cái khó ló cái khôn
Phê duyệt đề cương thử nghiệm lâm sàng từng giai đoạn, giám sát, kiểm tra, kết luận các báo cáo nghiên cứu là nhiệm vụ chính của Hội đồng đạo đức trong nghiên cứu y, sinh học cấp quốc gia. Chủ tịch hội đồng, GS Trương Việt Dũng cho hay đã nắm được tình hình ứng viên Covivac.
“Mọi khó khăn đều có giải pháp. Bên IVAC đã gọi điện thoại cho tôi, cho biết đang cân nhắc thiết kế đề cương giai đoạn 3 theo hướng nghiên cứu tính sinh miễn dịch, hiệu quả bảo vệ của Covivac như là mũi 3, liều tăng cường” - GS Dũng nói.
Cho đến thời điểm này, vấn đề tiêm mũi 3 tăng cường khoảng 6-8 tháng sau khi hoàn tất hai liều vaccine COVID-19 ban đầu đã được nhiều nước đặt ra và triển khai trên thực tế. Tương tự như mũi 2, liều bổ sung có thể theo hình thức tiêm trộn, mũi 3 có thể khác với hai mũi trước.
Thử nghiệm giai đoạn 3 Covivac tới đây có thể theo cách ấy: Tuyển tình nguyện viên là những người đã tiêm đủ hai mũi vaccine AstraZeneca, ở thời điểm cần phải tiêm tăng cường mũi 3 theo hướng dẫn của Bộ Y tế. Trong số này, một bộ phận sẽ được tiêm AstraZeneca, phần còn lại thì tiêm vaccine nghiên cứu Covivac. Sau đó sẽ thu thập dữ liệu để so sánh cả về tính an toàn, tính sinh miễn dịch và hiệu quả bảo vệ.
“Làm theo cách này sẽ rất thuận lợi. Tất nhiên cần tiền để đầu tư. IVAC là đơn vị nhà nước thì Nhà nước phải có trách nhiệm” - GS Dũng nhận xét.
Ông Hoàng Hoa Sơn cũng nghĩ vậy: “Điều cần thiết bây giờ là quyết liệt. Chúng tôi đang thúc IVAC sớm có báo cáo giữa kỳ giai đoạn 2, về tính sinh miễn dịch và liều sử dụng. Có vậy mới bàn đề cương giai đoạn 3 được. Còn nguồn vốn thì nếu dự án khả thi, chả nhẽ Nhà nước lại từ chối”.
| Thủ tướng đã chỉ đạo từ tháng 7 Từ tháng 7, khi làm việc với Tổ công tác đặc biệt của Chính phủ tại TP.HCM, Thủ tướng Phạm Minh Chính đã giao Bộ KH&CN phối hợp với Bộ Tài chính xem xét kinh phí nghiên cứu, thử nghiệm lâm sàng giai đoạn 3 ứng viên Covivac nhằm bảo đảm tính khả thi của việc nghiên cứu, thử nghiệm lâm sàng vaccine này. Ngoài ra, Thủ tướng cũng yêu cầu Bộ Tài chính chủ trì, phối hợp với Bộ Y tế xây dựng quy định cụ thể tiêu chuẩn, quy trình, định mức hỗ trợ việc nghiên cứu, sản xuất vaccine và kinh phí đầu tư nâng cấp quy mô sản xuất vaccine phòng COVID-19 trong nước từ các nguồn kinh phí hợp pháp; bảo đảm rõ ràng, công bằng, bình đẳng đối với tất cả đơn vị tham gia nghiên cứu. |