Thay vì xem xét cấp đăng ký lưu hành có điều kiện theo kết quả thử nghiệm lâm sàng giữa kỳ giai đoạn 3, với dữ liệu thu thập ở thời điểm ngày 2-9, Bộ Y tế mới đây đã yêu cầu Nanogen báo cáo bổ sung kết quả mới nhất của quá trình thử nghiệm này.
Nanogen là hãng dược tư nhân đang phát triển vaccine phòng COVID-19 Nano Covax, cùng Học viện Quân y và Viện Pasteur TP.HCM là hai tổ chức nhận thử nghiệm lâm sàng.
Báo cáo này phải gửi chậm nhất ngày 24-11 nhưng do cần thời gian thu thập hồ sơ gốc, phân tích, luận giải dữ liệu nên Học viện Quân y - đầu mối công tác thử nghiệm lâm sàng đã đề nghị lùi đến ngày 29-11. “Tuy nhiên, ngay cả mốc thời gian này cũng có thể không kịp” - tin từ Bộ Y tế và Học viện Quân y cho biết.
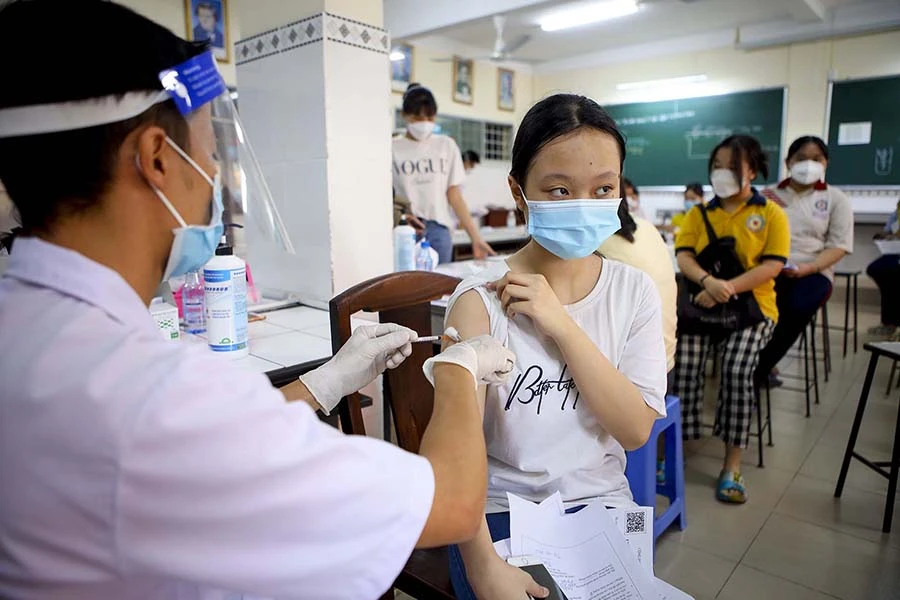
Người dân TP.HCM tiêm vaccine ngừa COVID-19. Ảnh: NGUYỆT NHI
| Căn cứ pháp lý Trong tình trạng cấp bách của đại dịch COVID-19, Thông tư 11 của Bộ Y tế ngày 19-8-2021 cho phép cấp đăng ký lưu hành có điều kiện với vaccine phòng COVID-19 thử nghiệm lâm sàng trong nước khi có đánh giá giữa kỳ giai đoạn 3 về tính an toàn và hiệu quả bảo vệ. Trong đó, hiệu quả bảo vệ có thể được ước tính trên cơ sở dữ liệu từ phòng thí nghiệm về tính sinh miễn dịch của vaccine thử nghiệm, chứ không đợi đến khi chứng minh trực tiếp bằng ca bệnh - vốn có thể cần nhiều thời gian, thậm chí là không thể “bắt” đủ nếu Việt Nam phòng dịch tốt như trước khi xuất hiện đợt dịch thứ tư. Việc ước tính này là thách thức rất lớn, bởi chuẩn mực của phát triển vaccine là phải tính toán trực tiếp hiệu quả bảo vệ trên cơ sở số trường hợp mắc bệnh trong nghiên cứu, thường được gọi là bắt ca bệnh. Chính vì vậy, ngày 11-11, Bộ Y tế đã ra Quyết định 5259 ban hành hướng dẫn chuyên môn chi tiết về xem xét tính an toàn, hiệu quả bảo vệ phục vụ đánh giá kết quả giữa kỳ thử nghiệm lâm sàng giai đoạn 3 với vaccine phòng COVID-19 sản xuất trong nước. |
Dữ liệu quan trọng: F0 trong tình nguyện viên
Chưa có báo cáo chính thức nhưng thông tin ban đầu mà chúng tôi nắm được là thử nghiệm lâm sàng trên người với vaccine Nano Covax đến thời điểm này đã thu được những dữ liệu quan trọng, nhất là xuất hiện một số lượng đáng kể F0 trong số hơn 14.000 tình nguyện viên (TNV) tham gia thử nghiệm. Đây là cơ sở trực tiếp để giúp tính toán hiệu quả bảo vệ của vaccine nói chung, trong đó có vaccine phòng COVID-19.
Việc thử nghiệm lâm sàng vaccine Nano Covax được thiết kế theo phương pháp truyền thống, với một số lượng nhất định TNV được tiêm vaccine thử nghiệm, một số lượng khác được tiêm giả dược (placebo) để so sánh đối chứng. Tất cả được “làm mù” - tức đánh mã số để đảm bảo bí mật, khách quan, ngẫu nhiên.
Khi xuất hiện một lượng nhất định ca nhiễm trong số TNV thì tổ chức thử nghiệm lâm sàng sẽ tiếp cận hồ sơ các ca nhiễm ấy từ các cơ sở y tế, bệnh viện dã chiến điều trị bệnh nhân COVID-19. Các ca F0 này sẽ được sàng lọc để đưa vào danh sách những trường hợp đủ điều kiện, như đã được tiêm đủ hai mũi, cách nhau đúng 28 ngày và thời điểm nhiễm là sau 14 ngày kể từ khi tiêm mũi 2… Sau đó sẽ tiến hành giải mù để xác định bao nhiêu F0 là sử dụng giả dược, bao nhiêu là được tiêm vaccine thử nghiệm. Trên cơ sở đó sẽ tính toán trực tiếp hiệu quả bảo vệ của vaccine thử nghiệm.
24, 48 và 69
Đề cương thử nghiệm vaccine Nano Covax đưa ra ba mốc tính toán, gắn với ba thời điểm bắt được 24, 48 và 69 ca nhiễm trong số TNV.
Trên thực tế, dữ liệu thử nghiệm lâm sàng vaccine Nano Covax ở thời điểm ngày 18-8, khi lập báo cáo giữa kỳ giai đoạn 3a, đã ghi nhận bảy ca mắc COVID-19. Nhưng con số ấy là quá ít so với yêu cầu trong đề cương. Đến thời điểm ngày 2-9, số ca mắc nhiều hơn nhưng vẫn chưa đạt số lượng tối thiểu. Từ đó đến nay gần ba tháng, với sự bùng phát dịch ở các tỉnh phía Nam cũng như tình hình F0 gia tăng ở các tỉnh phía Bắc mấy tuần gần đây thì số TNV tham gia thử nghiệm vaccine Nano Covax nhiễm COVID-19 đã tăng lên đáng kể.
“Số liệu thô là nhiều hơn cả số ca nhiễm đề cương yêu cầu. Nhưng đang trong quá trình thu thập, phân tích hồ sơ nên chưa biết sẽ có bao nhiêu F0 đủ điều kiện đưa vào danh sách chính thức” - nguồn tin cho biết.
Với các dữ liệu mới nhất này, chắc chắn báo cáo bổ sung kết quả thử nghiệm lâm sàng giữa kỳ giai đoạn 3 của vaccine Nano Covax sẽ đầy đủ, thuyết phục hơn rất nhiều so với báo cáo giữa kỳ giai đoạn 3 mà Hội đồng Đạo đức trong nghiên cứu y sinh học quốc gia họp, đánh giá hôm 18-9.
Báo cáo lúc ấy mới chỉ chứng minh được tính an toàn ngắn hạn của ứng viên vaccine Nano Covax trên dữ liệu bảy ngày sau tiêm mũi 1 của 11.430 TNV, kết quả theo dõi bảy ngày sau tiêm mũi 2 của 5.785 TNV. Cùng với đó là tính sinh miễn dịch.
Và điểm mấu chốt nhất lúc ấy là chưa có dữ liệu để đánh giá trực tiếp hiệu lực bảo vệ dựa trên số trường hợp mắc COVID-19 trong nghiên cứu. Mà chưa khẳng định được hiệu lực bảo vệ ở mức độ tối thiểu thì sẽ rất khó cho việc cấp phép lưu hành, kể cả lưu hành có điều kiện.
| Thủ tướng: Sản xuất bằng được thuốc và vaccine Sáng 27-11, tại trụ sở Chính phủ, Thủ tướng Phạm Minh Chính, Trưởng Ban chỉ đạo quốc gia về phòng chống dịch COVID-19, chủ trì cuộc họp về nhập khẩu và sản xuất vaccine, thuốc điều trị COVID-19 trong nước. Thủ tướng đặc biệt nhấn mạnh cần tháo gỡ mọi khó khăn, vướng mắc để thúc đẩy sản xuất bằng được vaccine và thuốc trong nước nhưng phải đảm bảo an toàn, khoa học, hiệu quả và đảm bảo công khai, minh bạch, chống mọi tiêu cực, sách nhiễu, lợi ích nhóm, cạnh tranh không lành mạnh trên cơ sở theo đúng quy định và phù hợp với điều kiện thực tế Việt Nam. Đây là những yêu cầu rất khắt khe. Thủ tướng yêu cầu các cơ quan, đơn vị, cá nhân có liên quan cần làm việc với tinh thần trách nhiệm cao nhất, không chịu bất cứ một tác động, sức ép nào. Các cơ quan quản lý, chuyên môn cần làm việc công tâm, khách quan, trung thực, hiệu quả để đạt mục tiêu của Đảng, Nhà nước, Chính phủ, Thủ tướng đề ra, đảm bảo các yêu cầu về chuyên môn, kỹ thuật. Thủ tướng đề nghị các nhà khoa học, các chuyên gia, các đơn vị nghiên cứu, sản xuất cần kiên trì theo đuổi công việc này vì mục tiêu khoa học, tinh thần nhân đạo và bảo vệ sức khỏe, tính mạng nhân dân. Tính mạng và sức khỏe của nhân dân là quan trọng nhất. Bộ Y tế, các bộ, ngành liên quan cần khẩn trương rà soát lại, hoàn thiện thể chế, hành lang pháp lý, bổ sung các cơ chế, chính sách cần thiết để hỗ trợ, thúc đẩy sản xuất thuốc và vaccine trong nước… |
































