Thực hiện quy định của Chính phủ, ngày 2-6, Cục Quản lý Dược (Bộ Y tế) đã có thông báo gửi các cơ sở đăng ký, cơ sở sản xuất thuốc lưu hành tại Việt Nam về việc công bố danh mục thuốc theo quy định tại khoản 1 Điều 14 Nghị định số 29/2022/NĐ-CP của Chính phủ.
Theo đó, Cục Quản lý dược thông báo công bố danh mục các thuốc, nguyên liệu làm thuốc sản xuất trong nước; Danh mục các thuốc, nguyên liệu làm thuốc nước ngoài; Danh mục các vaccine, sinh phẩm…
Các danh mục thuốc được đăng tải trên Cổng thông tin điện tử của Bộ Y tế tại địa chỉ: https://moh.gov.vn/home và Trang thông tin điện tử của Cục Quản lý Dược tại địa chỉ: https://dav.gov.vn.
Đơn vị này cho biết, các danh mục sẽ được tiếp tục cập nhật, bổ sung tại các đợt công bố tiếp theo.
 |
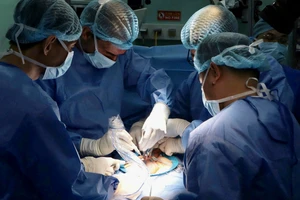
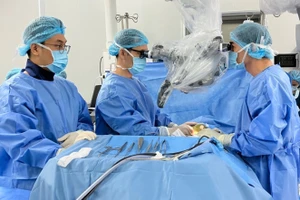
Cán bộ, chuyên viên của Cục Quản lý dược tất bật xử lý hồ sơ đăng ký lưu hành thuốc sắp hết hạn. Ảnh: NL |
Trước đó, chủ động ứng phó diễn biến phức tạp của dịch COVID-19 trong năm 2020-2021, Ủy ban Thường vụ Quốc hội từ ngày 30-12-2021 đã ban hành Nghị quyết số 12/2021/UBTVQH15 về việc cho phép thực hiện một số cơ chế, chính sách trong lĩnh vực y tế để phục vụ công tác phòng, chống dịch COVID-19.
Cụ thể, Khoản 5 Điều 6 của Nghị quyết này quy định: Đối với giấy đăng ký lưu hành thuốc, nguyên liệu làm thuốc hết hiệu lực trong khoảng thời gian từ ngày Nghị quyết này có hiệu lực đến trước ngày 31-12-2022 mà không thể thực hiện kịp thời thủ tục gia hạn đăng ký lưu hành do ảnh hưởng của dịch COVID-19 thì được tiếp tục sử dụng đến hết ngày 31-12-2022 để bảo đảm phục vụ công tác khám bệnh, chữa bệnh.
Ngày 29-4-2022, Phó Thủ tướng Chính phủ Vũ Đức Đam đã ký ban hành Nghị định 29/2022/NĐ-CP “Quy định chi tiết và biện pháp thi hành Nghị quyết số 12/2021/UBTVQH15 ngày 30-12-2021 của Ủy ban Thường vụ Quốc hội về việc cho phép thực hiện một số cơ chế, chính sách trong lĩnh vực y tế để phục vụ công tác phòng, chống dịch COVID-19”.
Trong đó Khoản 1 Điều 14 của Nghị định quy định Bộ Y tế có trách nhiệm công bố trên Cổng thông tin điện tử của Bộ Y tế Danh mục các thuốc, nguyên liệu làm thuốc có giấy đăng ký lưu hành hết hiệu lực trong khoảng thời gian từ ngày Nghị quyết số 12/2021/UBTVQH15 có hiệu lực đến trước ngày 31-12-2022 nhưng do ảnh hưởng của đại dịch COVID-19 nên chưa thể hoàn thành thủ tục gia hạn đăng ký lưu hành thì được tiếp tục sử dụng đến hết ngày 31-12-2022.
Về việc thực hiện Khoản 5 điều 6 Nghị quyết 12/2021 của UBTVQH15, trả lời phỏng vấn PLO, TS Nguyễn Văn Lợi, Trưởng phòng Đăng ký thuốc, Cục Quản lý Dược, Bộ Y tế cho biết, hiện tại, việc cung ứng thuốc cơ bản vẫn đảm bảo đầy đủ, chưa có bất thường gì cả, trong đó việc cấp phép vaccine COVID-19, cấp phép thuốc điều trị COVID-19 nhiều thủ tục đã được rút gọn nhưng vẫn đảm bảo quản lý chặt chẽ.
Ông Lợi cũng cho biết, hồ sơ cấp đăg ký lưu hành thuốc rất phức tạp, chưa kể hiện nay, nhiều cán bộ, công chức ở đơn vị đã xin thôi việc, nghỉ việc hoặc chuyển công tác dẫn đến năng suất, hiệu quả công việc giảm sút, khó đảm bảo tiến độ công việc...
“Từ tháng 6-2020, Cục Quản lý dược đã đưa vào khai thác hệ thống thẩm định trực tuyến. Đến nay, các thủ tục cơ bản trong đăng ký thuốc đã thực hiện nộp hồ sơ, thẩm định và trả kết quả trên hệ thống trực tuyến.
Hệ thống sẽ tiếp tục nâng cấp để tự động hóa cao hơn. Công việc quản lý cấp phép nhờ vậy sẽ mạch lạc, rõ ràng và nhanh hơn nhiều. Các việc như trả nhãn thuốc, hướng dẫn sử dụng, công bố nguyên liệu phục vụ nhập khẩu, sản xuất thuốc… tiến tới thực hiện nhanh chóng trên hệ thống trực tuyến thay cho cách làm thủ công bằng bản giấy như trước đây” – ông Lợi cho hay.