Hồ sơ này gồm nhiều hợp phần, trong đó các báo cáo về sản xuất, về quản lý chất lượng… đã được Hội đồng Tư vấn về cấp giấy đăng ký thuốc, nguyên liệu làm thuốc nghiên cứu trước đó theo quy trình cuốn chiếu, góp phần rút ngắn thời gian xử lý hồ sơ. Những phần còn lại, quan trọng nhất là cần đợi ý kiến của Hội đồng Đạo đức trong nghiên cứu y, sinh học quốc gia.
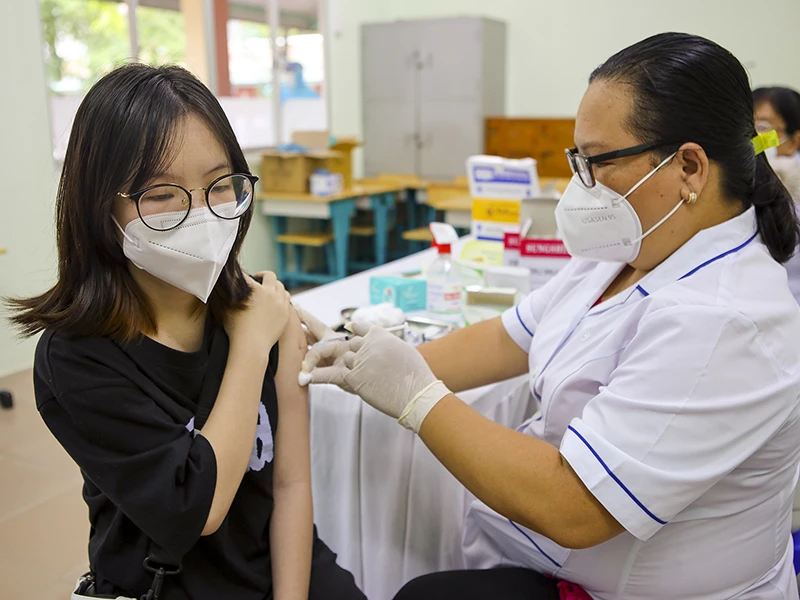
Nanogen đã gửi hồ sơ xin cấp phép trong trường hợp cấp bách cho ứng viên vaccine phòng COVID-19 Nano Covax. Trong ảnh: Người dân TP.HCM tiêm vaccine phòng COVID-19. Ảnh: NGUYỆT NHI
| Trong thời gian tới, Học viện Quân y, Viện Pasteur TP.HCM cùng nhà phát triển Nanogen tiếp tục xác minh các trường hợp mắc COVID-19 tính đến hết ngày 13-12 của chương trình thử nghiệm lâm sàng Nano Covax. Thông tin ban đầu là có hơn 170 trường hợp như vậy, vượt yêu cầu về số lượng theo đề cương nghiên cứu đã được phê duyệt. |
Về nội dung này, hội đồng đạo đức cuối tuần trước, hôm 16-12, đã họp xem xét báo cáo cập nhật, bổ sung kết quả thử nghiệm lâm sàng giai đoạn 3 Nano Covax. Kết quả cho thấy các dữ liệu mới nhất, tính đến ngày 30-11 đã củng cố các phân tích, đánh giá trước đó của hội đồng đạo đức tại cuộc họp hôm 18-9, vốn mới chỉ đánh giá dữ liệu chốt tới ngày 2-9.
Cụ thể, về tính an toàn, 12/12 phiếu của hội đồng đạo đức xác nhận đạt yêu cầu. Về tính sinh miễn dịch, 11/12 phiếu đánh giá đạt yêu cầu theo Quyết định 5259 của Bộ Y tế. Đây là hướng dẫn chuyên môn cụ thể nhất làm căn cứ xem xét cấp đăng ký lưu hành trong trường hợp cấp bách theo Thông tư 11 của Bộ Y tế. Một phiếu còn lại đánh giá đạt yêu cầu nhưng cần hoàn thiện báo cáo.
Điểm đáng chú ý nhất của cuộc họp này là quá trình thử nghiệm lâm sàng diện rộng Nano Covax giai đoạn 3, quy hơn 13.000 tình nguyện viên, đã thu được những dữ liệu ban đầu để có thể tính toán trực tiếp hiệu quả bảo vệ.
Cụ thể, chốt đến ngày 30-11, Học viện Quân y và Viện Pasteur TP.HCM - hai tổ chức nhận thử nghiệm lâm sàng Nano Covax đã xác định được 31 ca bệnh COVID-19. Kết quả mở mù để nghiên cứu hồ sơ y tế, cho thấy hầu hết các trường hợp này xuất hiện ở những tình nguyện viên tiêm giả dược. Qua đó tính toán trực tiếp được hiệu quả bảo vệ của Nano Covax theo dữ liệu ngày 30-11 là 56,2%.
Các ca nhiễm này hầu hết xảy ra ở thời điểm khoảng bốn tháng sau khi tình nguyện viên tham gia thử nghiệm. Do đó, trong tương quan so sánh các vaccine khác đã được cấp phép, hiệu lực bảo vệ đều suy giảm theo thời gian, thì con số 56,2% của Nano Covax không phải là thấp. Tuy nhiên, do số ca nhiễm “bắt được” còn ít nên khoảng tin cậy, theo ngôn ngữ chuyên môn của hội đồng đạo đức là còn rộng, cần tiếp tục đánh giá khi có dữ liệu đầy đủ hơn.
Điều này thể hiện rõ qua kết quả bỏ phiếu đánh giá hiệu quả bảo vệ trực tiếp của ứng viên Nano Covax: Hai phiếu đánh giá đạt yêu cầu; bốn phiếu đánh giá đạt yêu cầu nhưng cần hoàn thiện báo cáo; sáu phiếu đánh giá cần tiếp tục bổ sung dữ liệu các ca mắc COVID-19; và không có phiếu nào chấm vào ô “không đạt yêu cầu”.
| Nanogen có thể gửi hồ sơ xin xem xét Chủ tịch hội đồng đạo đức - GS Trương Việt Dũng chúc mừng Nanogen và hai tổ chức nhận thử nghiệm lâm sàng khi đã đưa dự án Nano Covax tới gần đích khoa học. Ông đánh giá đến lúc này, Nanogen hoàn toàn có thể gửi hồ sơ xin xem xét cấp đăng ký lưu hành trong trường hợp cấp bách với Nano Covax theo quy trình của Thông tư 11. Thông tư này cho phép Bộ Y tế cấp đăng ký lưu hành vaccine phòng COVID-19 khi mới có đánh giá giữa kỳ thử nghiệm lâm sàng giai đoạn 3, với hiệu quả bảo vệ là ước tính dựa trên tính miễn dịch, chứ chưa cần tính toán trực tiếp trên ca bệnh. |