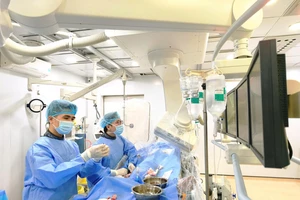
Trong khi chương trình tiêm chủng quốc gia chưa đáp ứng đầy đủ nhu cầu vaccine phòng bệnh, nhiều người dân đã tìm đến các điểm tiêm dịch vụ vaccine “5 trong 1” (Pentaxim do hãng Sanofi Pasteur, Pháp sản xuất), vaccine “6 trong 1” (Infanrix Hexa do GlaxoSmithKline, Anh sản xuất). Tuy nhiên, hai năm qua, hai loại vaccine này được nhập và phân phối nhỏ giọt rồi đột ngột dừng hẳn khiến những đứa trẻ đã tiêm các mũi trước đó phải mỏi mòn chờ vaccine này!
Đây là thực trạng quản lý vaccine nói riêng và thuốc chữa bệnh nói chung được đặt ra tại hội thảo góp ý dự án Luật Dược (sửa đổi) do Đoàn đại biểu Quốc hội TP.HCM tổ chức cuối tuần qua.
Công ty dược nước ngoài nắm đằng cán
“Đây là cuộc chơi mà phía công ty dược nước ngoài nắm đằng cán, các cơ quan chức Việt Nam nắm đằng lưỡi, còn thiệt hại là người dân vì chạy đôn chạy đáo tìm vaccine này, thậm chí đưa con ra nước ngoài để tiêm với giá cao” - một đại biểu nhận xét.
“Các công ty dược độc quyền đã quá xem thường sức khỏe trẻ em Việt Nam khi bỏ rơi những trẻ tiêm chưa đủ liều. Cơ quan quản lý ở đâu, tại sao sức khỏe của nhân dân mà cứ để thị trường điều chỉnh cung-cầu… Nói cho cùng, hiện ta không có luật để quy định, ràng buộc họ làm theo”.
Với thực trạng nêu trên, BS Trần Văn Khanh, Giám đốc BV quận 2 (TP.HCM), kiến nghị Luật Dược sửa đổi cần có quy định chống độc quyền, phá vỡ thế độc quyền để có thể cung cấp thuốc đầy đủ cho người dân khi cần, ngăn ngừa tình trạng khan hiếm như hai loại vaccine trên. Đặc biệt, BS Khanh nhấn mạnh việc cần ưu tiên, tạo chính sách khuyến khích, hỗ trợ công ty trong nước sản xuất thuốc tiêm ngừa vì trong nước đang rất thiếu.

Thuốc nội khó khăn tìm đường ra nước ngoài, trong khi thuốc ngoại vào Việt Nam quá dễ dàng. Ảnh: TÙNG SƠN
Bắt tay, lòng vòng nâng giá
Đại diện cho Hội Dược học TP.HCM, PGS-TS Phạm Khánh Phong Lan cho rằng về vấn đề quản lý giá thuốc, dự án luật có một chương riêng nhưng vẫn lặp lại những biện pháp chưa phát huy tác dụng, cũng “đẩy qua đẩy lại” trách nhiệm giữa các bộ. “Cần nhìn vào thực tế là giá thuốc có ba vấn đề chính mà phải thừa nhận là chưa kiểm soát được nó” - bà Lan nói.
Thứ nhất, cần làm rõ có tình trạng độc quyền thuốc và bắt tay nâng giá không. Theo bà Lan, bài học lớn nhất là từ Công ty Roche với thuốc Tamiflu (khi dịch bệnh xảy ra vào năm 2005, giá thuốc công ty này bán chỉ có 403.000 đồng/hộp nhưng bị thị trường đẩy lên tới 600.000-700.000 đồng/hộp). Tại Ấn Độ, trong những trường hợp dịch bệnh xảy ra, giá thuốc độc quyền bị đẩy lên quá cao thì doanh nghiệp Ấn Độ có quyền làm thuốc generic (thuốc hết hạn bảo hộ độc quyền). Do vậy luật nước ta cần có những điều khoản tương tự.
Thứ hai, tình trạng thuốc bán lòng vòng đẩy giá lên cao trước khi tới người bệnh. Theo bà Lan, trong nước có hơn 1.000 công ty TNHH dược, hệ thống công ty nhập khẩu, ủy thác từ ngoài về, sau đó đến các công ty trung gian, cuối cùng mới đến tay người dân thì giá thuốc đã đội lên rất cao.
Thứ ba, có điều khoản hạn chế tình trạng bắt tay giữa dược sĩ, bác sĩ kê thuốc ăn hoa hồng. “Đó là ba vấn đề lớn làm tăng giá thuốc mà Luật Dược sửa đổi cần giải quyết” - bà Lan nhấn mạnh.
Nhập thuốc vào quá dễ dàng
Ông Huỳnh Thành Lập, Trưởng Đoàn đại biểu Quốc hội TP.HCM, cho rằng cần có cơ chế kiểm tra tại nhà máy sản xuất đối với thuốc nhập khẩu. Theo ông Lập, hiện nay các nước trước khi nhập khẩu thuốc họ cử cán bộ đến các nước xuất khẩu để điểm tra, đánh giá, quyết định việc nhập khẩu. Chi phí này được các nước xuất khẩu chịu. Thực ra đây cũng là hàng rào kỹ thuật. Cũng theo ông Lập, hiện nay doanh nghiệp dược Việt Nam có thuốc xuất khẩu phải chịu chi phí cho các đoàn kiểm tra đến từ các nước nhập khẩu thuốc. Ngược lại, Việt Nam nhập khẩu nhiều loại thuốc nhưng lại chưa có quy định đến các nước kiểm tra quy trình sản xuất, như vậy là chưa bình đẳng và khó kiểm soát nguồn cung cấp cũng như chất lượng thuốc nhập khẩu.
“Trong phát triển công nghiệp dược thì làm sao ưu tiên phát triển ngành dược trong nước, chứ không để một thị trường mà có quá nhiều thuốc nhập khẩu. Tại sao thuốc chúng ta xuất khẩu thì cực khổ còn người ta nhập vào mình thì tương đối dễ dàng? Bao nhiêu năm qua chỉ có một đoàn duy nhất đến một nhà máy ở Ấn Độ để kiểm tra là vô lý” - bà Lan nói.
Tại hội thảo, nhiều đại biểu than phiền Cục Quản lý dược - Bộ Y tế chậm chạp trong việc đưa giá trần, giá sàn thuốc lên mạng. TS-BS Nguyễn Thanh Hùng, Giám đốc BV Nhi đồng 1, góp ý: “Dự thảo Luật Dược sửa đổi quy định việc công bố thông tin bán buôn, bán lẻ thuốc kê khai trên trang điện tử Bộ Y tế. Tuy nhiên, chúng tôi đề nghị định kỳ mỗi quý công bố giá thuốc kê khai trên trang điện tử”.
“Nói về công khai giá thuốc, thực tế Cục Quản lý dược chưa làm đủ hết các vấn đề đó (công khai giá trần, giá sàn trên cổng thông tin điện tử để các bệnh viện biết - PV). Nếu ghi luôn giá trên hộp thuốc thì vấn đề đấu thầu của các bệnh viện sẽ rất dễ dàng” - đại diện Sở Tài chính TP.HCM có ý kiến.
| Kiểm tra xong, dân dùng xong thuốc kém chất lượng Một thực tế là khi các cơ quan chức năng phát hiện thuốc kém chất lượng và tiến hành thu hồi thì thuốc đã tiêu thụ nhiều và nó ảnh hưởng đến sức khỏe người dân. Do đó cần quy định bổ sung vào Luật Dược sửa đổi việc tạm ngưng lưu hành thuốc đó cho đến khi có kết quả kiểm nghiệm. Sau khi điều tra xong có thể hủy quyết định tạm dừng thu hồi (nếu đạt chất lượng) hoặc thu hồi tiêu hủy nếu kém chất lượng. Vấn đề này các nước trên thế giới đã làm. Bà NGÔ HOA LƯ, Giám đốc Trung tâm Kiểm nghiệm thuốc, |